PGD nedir?
-
Ürünün piyasaya arzı veya dağıtımı aşamasında veya ürün piyasada
iken, ürünün tabi olduğu teknik düzenlemeye uygun olarak üretilip
üretilmediğini ve güvenli olup olmadığını denetlemek veya
denetlettirmek, güvenli olmayan ürünlerin güvenli hale getirilmesini
sağlamak ve gerektiğinde yaptırımlar uygulanması amacıyla Bakanlık
tarafından yapılacak her türlü faaliyeti kapsar.
-
Uygun olmayan tıbbi cihazların, gerektiğinde tedbirler alınması
suretiyle mevzuata uyumunu sağlayan, yeni yaklaşım direktiflerinin
uygulanması için etkili bir araçtır.
-
PGD kapsamında, uygun olmayan ürünlerin piyasaya arzını önlemek
için üreticiler, tedarikçiler, OK, UDK ve Yetkili Otoriteler işbirliği
yapmalıdır.
-
Piyasa gözetiminin etkin olabilmesi için imkanlar, risk
ihtimalinin daha yüksek olduğu veya uygunsuzluğun daha sık
gerçekleşebileceği veya özel bir çıkarın söz konusu olduğu yerlerde
yoğunlaştırılmalıdır.

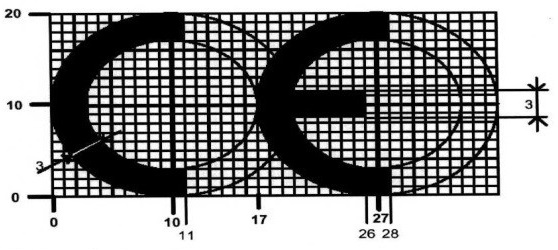
CE işareti nedir?
-
“CE” uygunluk işareti: “Community Europe” (Avrupa normlarına
uygunluk) “Üreticinin, ilgili teknik düzenleme/düzenlemelerden
kaynaklanan bütün yükümlülüklerini yerine getirdiğini ve ürünün ilgili
tüm uygunluk değerlendirme işlemlerine tabi tutulduğunu gösteren
işareti” ifade eder.
Tıbbi Cihaz PGD kapsamındaki ürün grupları nelerdir?
-
Tıbbi Cihazlar (93/42/EEC MD)
-
Vücuda yerleştirilebilir aktif tıbbi cihazlar, (90/385/EEC)
-
Vücut dışında kullanılan (in vitro) tıbbi tanı ürünleri, (98/79/EC IVDMD)
Tıbbi Cihazlarda AB, DSÖ, FDA vb ile İlişkiler:
-
Tıbbi cihazların denetimi kapsamında Avrupa Komisyonu bünyesinde
yürütmekte olan COEN- Uyum ve Uyumlaştırma Çalışma Grubu
(COEN-Compliance and Enforcement Group) üyesi olan Tıbbi Cihaz Denetim
Hizmetleri Daire Başkanlığımız bünyesindeki Tıbbi Cihaz Uluslararası
Koordinasyon ve Değerlendirme Birimi tarafından Avrupa Komisyonunca
yürütülen mevzuat çalışmaları takip edilmekte, denetim alanında
yürütülen çalışmalara katılım sağlamakta, sorunlu, güvensiz ürünler,
geri çekme, geri çağırma uygulanmış ürünlerle ilgili ortaklaşa çalışma
yürütülmekte, Avrupa Komisyonu ile ürün grupları ya da spesifik
ürünlerle ilgili e-mail, telekonferans yada toplantılar aracılığıyla
bilgi, görüş ya da veri paylaşımında bulunulmaktadır.
-
Ayrıca Avrupa Komisyonu haricinde FDA, Dünya Sağlık Örgütü gibi
diğer uluslararası kurum/kuruluşlar tarafından tıbbi cihazlar denetim
alanında yapılan tüm çalışmalar takip edilmekte ve söz konusu ülke,
kurum/kuruluşlar ile işbirliği sağlanmaktadır.”
PGD Kapsamında Yükümlülük ve Sorumluluklar:
-
Üretici, İthalatçı, Satıcıların sorumlulukları:
-
Üretici/ithalatçı, piyasaya sadece güvenli ürünleri arz etmek zorundadır.
-
Üretici/ithalatçı, teknik düzenlemede belirtilen tüm
belgeleri; bu belgeler kapsamındaki ürünün yurt içinde üretiliyor ise
üretildiği, ithal ise ithal edildiği tarihten itibaren muhafaza etmek ve
istenilmesi halinde yetkili kuruluşlara ibraz etmekle yükümlüdür.
-
Üretici/ithalatçı gerektiğinde piyasaya arz edilmiş
ürünlerden numuneler alarak test etmek, şikayetleri soruşturmak ve
yapılan denetim sonuçlarından dağıtıcıları haberdar etmek, riskleri
önlemek amacı ile ürünlerin toplatılması ve bertarafı da dahil olmak
üzere gerekli önlemleri almakla yükümlüdür.
-
Dağıtıcı, sahip olduğu bilgiler çerçevesinde, güvenli olmadığını bildiği ürünleri piyasaya arz edemez.
-
Dağıtıcı, faaliyetleri çerçevesinde, ürünlerin taşıdığı
riskler ve bu risklerden korunmak için alınması gereken önlemler
hakkında ilgililere bilgi verir.
-
Sağlık Kurum ve Kuruluşlarının sorumlulukları:
-
Satın alımlarda, ürünlerin Kurumumuz internet sayfasında
Güvensiz ürün olarak ilan edilip edilmediğinin kontrolünün yapılması,
-
Ürünlerin Kurumumuz veritabanında kayıtlı olup olmadığının kontrolünün yapılması,
-
Ürünlerde bir uygunsuzluk görüldüğünde, hem alınan firmaya hem de Kurumumuza bildirilmesi,
-
Vatandaşın sorumlulukları:
-
Menşei bilinmeyen, satış yeri belli olmayan yerlerden
telefon, TV, internet vb. kanallardan tıbbi cihaz alınmaması,
-
TİTUBB veri tabanında kayıtlı olmayan tıbbi cihazların alınmaması,
-
Üründe bir uygunsuzluk olduğunda Kurumumuza bildirilmesi,




